
โดย …ผศ.ดร.เนตรนภิส เขียวขำ ภาควิชาโรคพืช คณะเกษตร มหาวิทยาลัยเกษตรศาสตร์
ในการเกิดโรคพืชมีกระบวนการและปัจจัยที่เกี่ยวข้องบางอย่างที่มีส่วนในการทำให้เกิดโรค ปัจจัยเหล่านี้จะขาดปัจจัยหนึ่งปัจจัยใดไม่ได้ กล่าวคือ ถ้าขาดอย่างใดอย่างหนึ่งไปหรือมีไม่ครบถ้วน ลักษณะอาการของโรคพืชก็จะไม่แสดงให้เห็นหรือพืชไม่เป็นโรค ปัจจัยดังกล่าวประกอบด้วย เชื้อสาเหตุของโรค พืชอาศัย สภาพแวดล้อม และระยะเวลาในการเข้าทำลาย (สืบศักดิ์, 2554) การเข้าทำลายของเชื้อราสาเหตุโรคหลังการเก็บเกี่ยวหลายชนิด จะเริ่มจากอาศัยอยู่กับผลิตผลแบบแฝง (quiescent) ในระยะที่ผลเจริญเติบโตโดยไม่แสดงอาการให้เห็น เมื่อผลเข้าสู่ระยะสุกแก่และเสื่อมสภาพ เชื้อราสาเหตุโรคก็จะเข้าทำลายทำให้เกิดอาการของโรค เนื่องจากในระยะผลยังอ่อน พืชจะสร้างกลไกการป้องกันตัวเพื่อจำกัดการเจริญของเชื้อรา ต่อมาเมื่อผลสุกแก่กลไกการป้องกันตัวมีการเปลี่ยนแปลงทำให้เชื้อราสามารถเจริญได้ โดยในที่นี้จะขอกล่าวถึงผลกระทบของการเปลี่ยนแปลงค่าความเป็นกรดด่างในผลิตผลต่อเชื้อราสาเหตุโรคพืช ค่าความเป็นกรดด่างของผลิตผลที่เพิ่มหรือลดลง ส่งผลต่อการกลไกการป้องกันตัวของพืช ทำให้เชื้อราสาเหตุโรคถูกกระตุ้นให้มีการปลดปล่อยเอนไซม์ย่อยเนื้อเยื่อพืชอาศัย จึงก่อให้เกิดโรคได้ ความเป็นด่างจะเกิดจากปฏิกิริยาการผลิตแอมโมเนีย (ammonification) ในเนื้อเยื่อพืชที่มีการเข้าทำลายของเชื้อรา เช่น Colletotrichum และ Alternaria ส่วนความเป็นกรดเกิดจากปฏิกิริยาการสร้างกรด (acidification) ที่เป็นพวกกรดอินทรีย์ต่างๆ ในเนื้อเยื่อพืชที่มีการเข้าทำลายของเชื้อรา เช่น Penicillium Botrytis และ Sclerotinia (Pursky et al., 2010)
เชื้อราสาเหตุโรคหลังการเก็บเกี่ยวจะมีช่องทางการเข้าทำลายเนื้อเยื่อพืชอาศัยได้ 3 ลักษณะ ได้แก่ 1) การเข้าทำลายทางบาดแผลที่เกิดจากสิ่งมีชีวิต เช่น แมลงหรือสัตว์ และบาดแผลที่เกิดจากสิ่งไม่มีชีวิต เช่น เครื่องมือการเกษตร การกระแทก รอยแยกจากการพัฒนาของผล ในระหว่างการเจริญและการเก็บรักษา 2) การเข้าทางรอยเปิดตามธรรมชาติของพืชอาศัย เช่นเลนติเซล ขั้วผล ก้านผล และ 3) การเข้าโดยตรงที่บริเวณรอยแตกของชั้นคิวติเคิลในระยะที่มีการพัฒนาของผล

การเปลี่ยนแปลงค่าความเป็นกรด-ด่าง (pH) ของสิ่งแวดล้อมหรือพืชอาศัย มีผลต่อการเกิดโรคจากเชื้อราสาเหตุโรคหลังการเก็บเกี่ยว การเปลี่ยนแปลงค่า pH ทำให้เกิดการเพิ่มหรือลดปริมาณเชื้อราได้ซึ่งอธิบายได้จากการที่เชื้อรามีทั้งประเภทที่เป็นเชื้อราที่เจริญในสภาพด่าง (alkalizing fungi) และเชื้อราที่เจริญในสภาพกรด (acidifying fungi) ค่า pH ของพืชอาศัยที่เหมาะสมจะมีผลต่อการสร้างเอนไซม์ของเชื้อรา การเปลี่ยนแปลง pH ของพืชอาศัยมีความสำคัญในการกระตุ้นให้เชื้อราที่เข้าทำลายแบบแฝงสามารถเจริญและพัฒนาก่อโรคในพืชได้ เชื้อราที่เจริญในสภาพด่างเช่น ผลอะโวคาโดในระยะสุกแก่และเสื่อมสภาพ จะมีค่า pH เปลี่ยนแปลงเพิ่มขึ้นจาก 5.2 เป็น 6 ในระยะที่เข้าสู่การสุกแก่ (Yakoby et al., 2000) ในระหว่างเชื้อราสาเหตุโรคเพิ่มปริมาณในพืชอาศัยจะเกิดมีปฏิกิริยาการผลิตแอมโมเนียขึ้น เช่นเชื้อรา Colletotrichum และ Alternaria จะสร้างแอมโมเนียออกมา ในชั้น pericarp ของผลอะโวกาโดซึ่งมี pH 5.2 ทำให้ pH เพิ่มขึ้นเป็น 7.5-8 เช่นเดียวกับผลมะเขือเทศจะมี pH 4.1-4.5 เมื่อเชื้อรา C. gloeosporioides เข้าทำลาย บริเวณบาดแผลที่เน่าเสียมี pH เพิ่มขึ้นเป็น 8 และมีการสะสมแอมโมเนียเป็น 3.6 มิลลิโมลาร์ เมื่อเปรียบเทียบกับเนื้อเยื่อพืชปกติที่มีแอมโมเนีย 0.2 มิลลิโมลาร์ (Alkan et al., 2008; Prusky et al., 2001) เช่นเดียวกับ พริกหยวก แตงเมล่อน เชอร์รี่ และพลับ (Eshel et al., 2002) ที่พบการเข้าทำลายของเชื้อรา A. alternata จะมีความเข้มข้นแอมโมเนียเพิ่มขึ้น 3-10 เท่า และส่งผลให้ pH เพิ่มขึ้นจาก 0.2 เป็น 2.4 การสร้างแอมโมเนียนั้น เกิดจากกิจกรรมของเอนไซม์ย่อยโปรตีนและการย่อยกรดอะมิโน (Prusky and Yakoby, 2003) เมื่อผลไม้ที่มีความเป็นกรดถูกเชื้อราเข้าทำลาย เชื้อราจะสร้างแอมโมเนียออกมาเกิดสภาพด่างทำให้เชื้อรามีความรุนแรงในการก่อโรค การสะสมแอมโมเนียเป็นปัจจัยที่สำคัญในการเข้าทำลายของเชื้อรา Colletotrichum และทำให้เกิดการพัฒนาของโรคในผลิตผลสุก และพบการสร้างเอนไซม์ arsenal (Prusky and Yakoby, 2003) ซึ่งเป็นเอนไซม์ที่สร้างจากเชื้อสาเหตุโรคมีหน้าที่ย่อยสลายผนังเซลของพืช นอกจากนี้ยังมีการศึกษาการแสดงออกของ endoglucanase ยีน AaK1 ที่เกิดจากเชื้อรา Alternaria alternata จะเกิดขึ้นเมื่ออยู่ในสภาวะที่มีค่า pH มากกว่า 6 ในเนื้อเยื่อพืชที่มีการเน่าเสีย ซึ่ง endoglucanase เป็นเอนไซม์สร้างจากเชื้อรา แบคทีเรีย และโปโตรซัว มีหน้าที่เร่งปฏิกิริยาการย่อยสลาย cellulose ในผนังเซล ยีน AaK1 จะไม่แสดงออกเมื่ออยู่ในสภาวะ pH ต่ำ ทำให้อยู่ในสภาวะการเข้าทำลายแบบแฝง (Eshel et al., 2002) เชื้อรา Colletotrichum มียีน pelB ที่จะแสดงออกเมื่อค่า pH มากกว่า 5.7 (Yakoby et al., 2001)
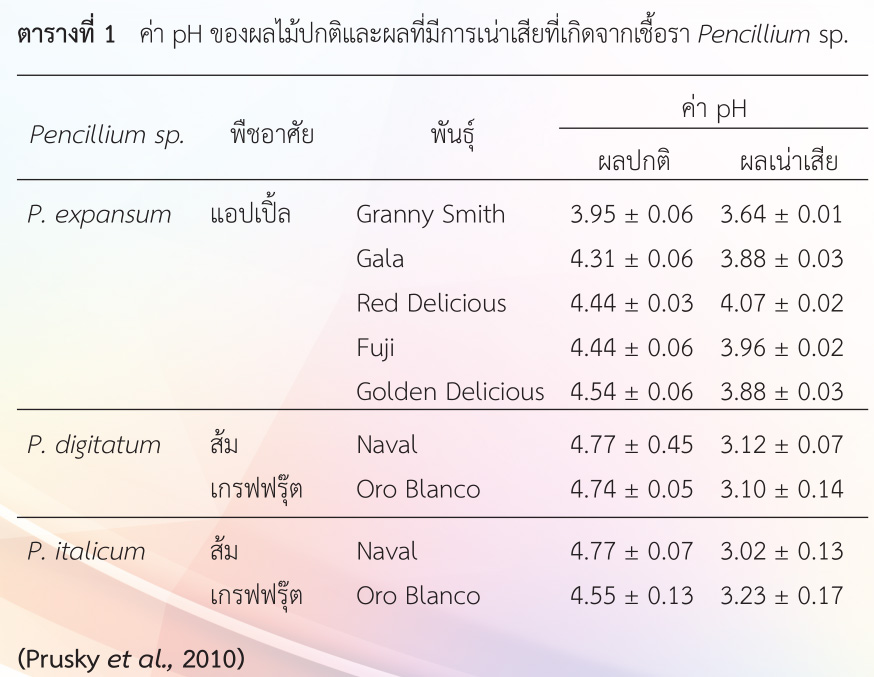
ส่วนเชื้อราที่เจริญในสภาพกรด ได้แก่เชื้อรา Pencillium expansum P. digitatum P. italicum B. cinerea และ Sclerotium sclerotiorum จะปลดปล่อยกรดอินทรีย์ทำให้เกิดสภาพความเป็นกรดในเนื้อเยื่อ เชื้อรา Pencillium spp. สร้างกรดเมื่อเข้าทำลายแอปเปิ้ลและส้ม ทำให้ผลแอปเปิ้ลมีค่า pH ลดลง จากปกติเนื้อเยื่อ mesocarb มีค่า pH ระหว่าง 3.95-4.31 ลดลงเป็น 3.64-3.88 ในเนื้อเยื่อพืชที่ถูกทำลาย (ตารางที่ 1) (Prusky et al., 2010) เชื้อรา S. sclerotiorum ในระหว่างเข้าทำลายพืชจะสร้างกรด oxalic ทำให้ค่า pH ของพืชลดต่ำลงเหลือเพียง pH 4 (Rollins and Dickman, 2011) ซึ่งการเกิดกรด oxalic เป็นสิ่งบ่งบอกว่ามีการเข้าทำลายของเชื้อในระหว่างการติดเชื้อ เช่น แบคทีเรียจะสร้างกรด oxalic ขึ้นเพื่อออกซิไดส์คาร์โบไฮเดรตของพืช ส่วนเชื้อรา Pencillium spp. และ Aspergillus สร้างกรด citric และ gluconic สะสมในเนื้อเยื่อพืช ซึ่งทำให้ค่า pH ลดลง 0.5-1 หน่วย และเกิดการกำจัดแอมโมเนียออกจากเนื้อเยื่อพืชทำให้ค่า pH ลดต่ำลง (Prusky and Yakoby, 2003; Ruijter et al., 1999)

ที่มา: ภาพ 3A http://www.viarural.com.ar/viarural.com.ar/agricultura/aa-enfermedades/penicillium-expansum-01.jpg, ภาพ 3B ศศิวิมล (2553)
เชื้อรา P. expansum เป็นเชื้อสาเหตุโรคผลเน่าในแอปเปิ้ล สร้างกรด gluconic สะสมในเนื้อเยื่อพืช ตรวจพบการแสดงออกของยีน gox2 สูง ซึ่งเป็นยีนที่มีหน้าที่ออกซิไดซ์กลูโคสและปลดปล่อยกรด gluconic (Hadas et al., 2007) การสะสมกรด gluconic และ oxalic เกิดขึ้นเมื่อพืชถูกเชื้อราเข้าทำลายซึ่งการเปลี่ยนแปลงของค่า pH เกี่ยวข้องกับการแสดงออกของยีน pac 1 (phosphatase of activated cells 1) ทำหน้าที่เป็นตัวกลางใน zinc finger transcription factor การเกิดกรด oxalic ยังเกิดขึ้นจากกิจกรรมเอนไซม์ oxaloacetase ที่สลาย oxaloacetate (Rollins and Dickman, 2001) การเปลี่ยนแปลงของค่า pH ในสิ่งแวดล้อมหรือผลิตผลเป็นปัจจัยที่เชื้อสาเหตุโรคเลือกเข้าทำลายที่มีความเฉพาะเจาะจงในพืชอาศัยแต่ละชนิด ในงานวิจัยที่กล่าวข้างต้นพบว่ายีนของเชื้อราจะถูกกระตุ้นจากการเปลี่ยนแปลงค่า pH ซึ่งยีนหลายชนิดทำให้เกิดการสร้างเอนไซม์ที่มาย่อยผนังเซลของพืช เชื้อรา P. expansum จะสร้างกรด gluconic และ citric ช่วยในการทำงานของเอนไซม์ที่ย่อยโปรตีน มีการทดลองเพิ่มความเป็นกรด pH 3-5 ในอาหารเลี้ยงเชื้อรา P. expansum ตรวจพบว่ามีการเพิ่มของยีน pepg1 (endopolygalacturanase gene) และในบริเวณเป็นด่างจากการเติม NaHCO3 พบการเจริญของเชื้อราลดลง (Prusky and Yakoby, 2003)
สิ่งที่มีผลให้การเข้าทำลายแบบแฝงพัฒนาให้เกิดการก่อโรค โดยการเปลี่ยนสถานะจากการอยู่ร่วมกัน (biotrophism) เป็นการก่อโรคหรือการย่อยสลาย (necrotropic-saprophytic stage) มีปัจจัยที่ทำให้เกิดกลไกดังกล่าวภายในเซลที่มีผลมาจากชนิดและปริมาณแร่ธาตุต่างๆ และค่า pH ที่เหมาะสม สารที่ถูกปลดปล่อยออกมา เช่น กรดอินทรีย์ เป็นส่วนสำคัญที่ทำให้เกิดการก่อโรคและทำให้เกิดความรุนแรงของโรคตามมาโดยมีการทำงานแบ่งเป็น 3 ลักษณะ ได้แก่ 1) การเกิดสาร oxalate ซึ่งจะเป็นพิษโดยตรงต่อพืชอาศัยหรือทำให้พืชอ่อนแอ 2) อาจมีการชะล้างแคลเซียมที่ผนังเซลเนื่องมาจากกรด oxalic และ gluconic ทำให้ผนังเซลอ่อนนิ่ม (Hadas et al., 2007) และ 3)สาร oxalate ไปยับยั้งการสร้าง Reactive oxygen species (ROS) ของพืช และขัดขวางกลไกการป้องกันตัวเองของพืช (Kim et al., 2008) การสร้างแอมโมเนียมีผลทั้งทางกายภาพและชีวเคมีต่อทั้งพืชและเชื้อสาเหตุโรค เนื้อเยื่อพืชปกติจะมีอิเล็กตรอนและโปรตรอนระหว่าง plasma membrane ซึ่งมีความสำคัญต่อการแลกเปลี่ยนไอออน การเคลื่อนที่ของของเหลว และการเจริญของผนังเซล ความเป็นพิษของแอมโมเนียจะทำให้พืชมีการสังเคราะห์เอทิลีนและมีการเปลี่ยนแปลงของการผ่านเข้าออกของสารในเซลเมมเบรน และส่งผลให้พืชมีการสะสมของ ROS เนื่องจากกลไกของ NADPH oxidase ทำให้เกิดบริเวณเนื้อเยื่อตาย (cell death) บนผลมะเขือเทศซึ่งส่งผลดีทำให้เป็นบริเวณจำกัดไม่ให้เส้นใยเจริญต่อไปได้ (Alkan et al., 2009)
ความซับซ้อนของการเข้าทำลายแบบแฝงเกี่ยวของกับการเปลี่ยนแปลงทางกายภาพ และชีวเคมีของพืชอาศัยในระหว่างการสุกและการเสื่อมสภาพอันนำไปสู่การอ่อนแอต่อโรค ประกอบกับเชื้อที่เข้าทำลายแบบแฝงมีความสามารถต้านทานสารยับยั้งเชื้อราในพืชอาศัยที่มีลดลงเมื่อเข้าสู่ระยะสุกแก่ได้ การเปลี่ยนแปลงทางกายภาพ อาทิเช่น ค่า pH ในเนื้อเยื่อพืชอาศัย ปริมาณน้ำตาล องค์ประกอบของผนังเซล หรือบาดแผล เหล่านี้ล้วนกระตุ้นให้เชื้อราเจริญได้ ความเป็นกรดในเนื้อเยื่อพืชจากกรดอินทรีย์ (oxalic และ gluconic) หรือความเป็นด่างจากการสร้างแอมโมเนีย อาจมีส่วนทำให้เนื้อเยื่อเน่าเสียอย่างรวดเร็วได้ รวมทั้งผลของการแสดงออกของยีนและการปลดปล่อยเอ็นไซม์พวกที่ย่อยผนังเซล การหาคำตอบของการเปลี่ยนแปลงสิ่งที่ส่งสัญญาณต่างๆ เช่น pH ไนโตรเจน และน้ำตาล ที่มีผลต่อการก่อโรคหลังการเก็บเกี่ยวในระยะที่ผลิตผลสุกแก่ยังคงต้องหาคำตอบต่อไป แต่อย่างไรก็ตามปัจจุบันเราทราบแล้วว่าค่า pH ของพืชอาศัยมีผลต่อการพัฒนาของเชื้อสาเหตุโรคอันจะนำไปสู่การควบคุมโรคในการศึกษาต่อไปในอนาคต (Prusky et al., 2006)
แนวทางในการแก้ปัญหาโรคหลังการเก็บเกี่ยวด้วยการเปลี่ยนแปลงค่าความเป็นกรดด่าง จากงานวิจัยที่ผ่านมามีการใช้กรดร่วมกับกรรมวิธีการอื่นๆ ในการจัดการโรคหลังการเก็บเกี่ยว เช่นการใช้น้ำส้ม (กรดอะซิติก) ความเข้มข้นร้อยละ 1-3 ในน้ำ อุณหภูมิ 50 องศาเซลเซียส สามารถลดการเจริญของสปอร์ของเชื้อรา Penicillium expansum สาเหตุโรคผลเน่าของแอปเปิ้ล โดยทดลองแช่ผลแอปเปิ้ล พันธุ์ Red Delicious ในกรดน้ำส้มที่อุณหภูมิดังกล่าว ความเข้มข้นร้อยละ 3 นาน 2 นาที สามารถลดอาการผลเน่าได้ (Radi et al., 2010) Venditti et al. (2009) ทดลองรมผลส้มแมนดารินด้วยไอของกรดน้ำส้มความเข้มข้น 75 ไมโครลิตรต่อลิตร นาน 15 นาที ที่อุณหภูมิ 36 องศาเซลเซียส ที่ความชื้นสัมพัทธ์ร้อยละ 95 พบว่าสามารถยับยั้งเชื้อรา Penicillium digitatum ที่ปลูกเชื้อบนผลส้มแมนดารินเก็บเกี่ยวใหม่ 2 พันธุ์ ได้แก่พันธุ์ Fremont และ Fairchild โดยพบการเน่าเสียเพียงร้อยละ 8.3 และ 2.1 ตามลำดับ นอกจากนี้ยังมีการทดลองพ่นกรดมะนาว (กรดซิตริก) ความเข้มข้น 1,000-2,000 ไมโครลิตรต่อลิตร เป็นเวลา 30 นาที มีผลในการฆ่าเชื้อจุลินทรีย์ที่ผิวผลสตรอเบอรี่ (Vardar et al., 2012)
** บทความนี้ตีพิมพ์ลงใน Postharvest Newsletter ปีที่ 18 ฉบับที่ 1 มกราคม – มีนาคม 2562
เอกสารอ้างอิง
- สืบศักดิ์ สนธิรัตน์. 2554. การจัดการโรคพืช. ภาควิชาโรคพืช มหาวิทยาลัยเกษตรศาสตร์. หจก. เกษมศรี ซี.พี. กรุงเทพฯ. 128 หน้า.
- ศศิวิมล ลักษณพิสุทธิ์. 2553. การควบคุมโรคผลเน่าราสีเขียว ที่เกิดจากเชื้อรา Penicillium digitatum Sacc. บนผลส้มพันธุ์สายน้ำผึ้ง ด้วยสารสกัดจากขมิ้นชัน (Turmeric ; Curcuma longa Linn.). วิทยานิพนธ์ปริญญาโท.บัณฑิตวิทยาลัย, มหาวิทยาลัยเกษตรศาสตร์. 133 หน้า.
- Alkan, N, R. Fluher, A. Sherman and D. Prusky. 2008. Role of ammonia secretion and pH modulation on pathogenicity of Colletotrichum coccodes on tomato fruit. Mol Plant Microbe Interact 21:1058-1066.
- Alkan, N., R. Fluhr, M. Sagi, O. Davydov and D. Prusky. 2009. Ammonia secreted by Colletotrichum coccodes effects host NADPH oxidase activity enhancing cell death and pathogenicity in tomato fruits. Molecular Plant-Microbe Interactions 22: In press
- Eshel, D., I. Miyara, T. Ailinng, A. Dinoor and D. Prusky. 2002. pH regulates endoglucanase expression and virulence of Alternaria alternata in persimmon fruits. Mol Plant Microbe Interaction 15:744-779.
- Hadas, Y., I. Goldberg, O. Pines and D. Prusky. 2007. The relationship between expression of glucose oxidase, gluconic accumulation, acidification of host tissue and the pathogenicity of Pencillium expansum. Phytopathology 97:384-390.
- Kim, K.S., J.Y. Min and M.B. Dickman. 2008. Oxalic acid is an elicitor of plant programmed cell death during Sclerotinia sclerotiorum disease development. Mol Plant Microbe Interact 21:605-612.
- Prusky, D. and N. Yakoby. 2003. Pathogenic fungi: leading or led by ambient pH? Mol Plant Pathol 4: 509-516.
- Prusky, D., J.L. McEvoy, B. Leverentz and W.S. Conway. 2001. Local modulation of host pH by Colletotrichum species as a mechanism to increase virulence. Mol Plant Microbe Interact 14:1105-1113.
- Prusky, D., I. Kobiler, M. Aderman and I. Miyara. 2006. Effect of acidic solutions and acid Prochloraz on the control of postharvest decays caused by Alternaria alternata in mango and persimmon fruit. Postharvest Biol Technol 42:134-141.
- Prusky, D., N. Alkan, I. Miyara, S. Barad, M. Davidzon, I. Kobiler, S. Brown-Horowitz, A. Lichter, A. Sherman and R. Fluhr. 2010. Mechanisms modulation postharvest pathogen colonization of decaying fruits. In D. Prusky and M.L. Gullino. Post-harvest pathology. Springer. pp.43-56.
- Radi, M., H.A. Jouybari, G. Mesbahi, A. Farahnaky and S. Amiri. 2010. Effect of hot acetic acid solutions on postharvest decay caused by Penicillium expansum on Red Delicious apples. Scientia Horticulturae 126: 421–425.
- Rollins, J.A. and M.B. Dickman. 2011. pH signaling in Sclerotinia sclerotiorum: identification of pacC/RIM1 homolog. Applied Environ Microbiol 67:75-81.
- Ruijter, G.J.G., P.J. van de Vondervoort, and J. Visser. 1999. Oxalic acid production by Aspergillus niger: an oxalate-non-producing mutant produces citric acid at pH 5 and in the presence of manganese. Microbiology 145:2569-2576.
- Vardar, C., K. Ilhan and O.A. Karabulut. 2012. The application of various disinfectants by fogging for decreasing postharvest diseases of strawberry. Postharvest Biology and Technology 66: 30–34.
- Venditti, T., A. Dore, M.G. Molinu, M. Agabbio and G. D’hallewina. 2009. Combined effect of curing followed by acetic acid vapour treatments improves postharvest control of Penicillium digitatum on mandarins. Postharvest Biology and Technology 54: 111–114.
- Yakoby, N., I. Kobler, A. Dinoor and D. Prusky. 2000. pH regulation of pectate lyase secretion modulates the attack of Colletotrichum gloeosporioides on avocado fruits. Appl Environ Microbiol 66:1026-1030.
- Yakoby, N., D. Beno-Moualem, N.T. Keen, A. Dinoor, O. Pines, and D. Prusky. 2001. Colletotrichum gloeosporioides pelB, is an important factor in avocado fruit infection., Mol Plant Microbe Interact 14: 988-995.



